Kationi vs. anioni
Sisältö
- Sisältö: Ero kationin ja anionin välillä
- Vertailutaulukko
- Mitä kationit ovat?
- Mitä anionit ovat?
- Keskeiset erot
- johtopäätös
Ero kationin ja anionin välillä on, että kationi sisältää siihen positiivisen varauksen, kun taas anionilla on negatiivinen varaus.
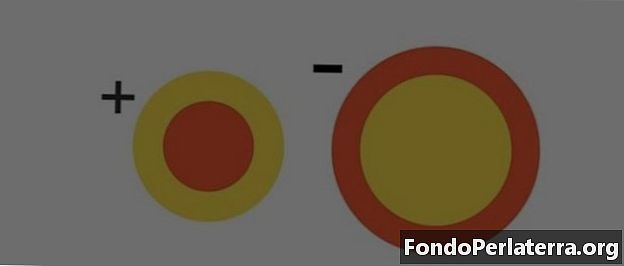
Kationi ja anioni ovat atomeja, joissa on varaus niihin. Täällä opitaan tuntemaan näiden varautuneiden hiukkasten erot. Kationit osoittavat niille positiivisen varauksen, kun taas anionien negatiivinen varaus.
Sana "kationi" on otettu kreikan sanasta "kata", joka tarkoittaa alaspäin. Vaikka sana anion on peräisin kreikan sanasta “ano”, joka tarkoittaa ylöspäin. Kationit vetoavat aina katodia kohti, joka on negatiivisesti varautunut elektrodi, kun taas anioneja vedetään aina kohti anodia, joka on positiivisesti varautunut elektrodi.
Kationit muodostuvat, kun atomi menettää yhden tai useamman elektronin, ja siten atomiin, josta tulee sitten kationi, ilmestyy positiivinen varaus. Anioni muodostuu, kun atomi saavuttaa yhden tai useamman elektronin ja muuttuu siten negatiivisesti varautuneeksi. Kationit muodostuvat metallien atomeista, kun taas anionit muodostuvat epämetallien alkuaineista. Kationeissa protonien lukumäärä on enemmän kuin elektronien lukumäärä, ja siksi se osoittaa positiivisen varauksen. Anionissa elektronien lukumäärä on suurempi kuin protoneissa, ja siksi niillä on negatiivinen varaus.
Kemiallisessa reaktiossa kationit reagoivat anionien kanssa muodostaen ionisen yhdisteen. Kationi ei voi koskaan reagoida kationin kanssa, ja anioni ei voi koskaan reagoida anionin kanssa. Kationin säde on aina suurempi kuin anionin säde, koska kationeissa kiertoradat menetetään elektronien menetyksen myötä, kun taas anioneissa kiertoradan lukumäärä kasvaa elektronien vahvistuksen myötä. Kationi, jolla on positiivinen varaus, merkitään ylämerkillä + yhdisteen elementin tai kemiallisen kaavan nimen jälkeen, esim. Fe2 + ja NH4 +. Anionia merkitään samalla tavalla yläindeksillä - elementin nimen tai yhdisteen kemiallisen kaavan jälkeen, esim. Br-N3- jne. Esimerkkejä kationeista ovat rauta (Fe2 + ja Fe3 +), natrium (Na + ), kalium (K +) ja magnesium (Mg2 +). Esimerkkejä anioneista ovat kloridi (Cl-), flouridi (F-), bromidi (Br-), hydridi (H-) ja nitridi (N-).
Sisältö: Ero kationin ja anionin välillä
- Vertailutaulukko
- Mitä kationit ovat?
- Mitä anionit ovat?
- Keskeiset erot
- johtopäätös
Vertailutaulukko
| Perusta | kationi | Anion |
| Määritelmä | Ne ovat tyyppiä hiukkasia, joilla on positiivinen varaus. | Ne ovat hiukkasia, joilla on negatiivinen varaus. |
| Miksi heillä on veloitus? | Heillä on positiivinen varaus, koska ne menettävät yhden tai useamman elektronin. | Heillä on negatiivinen varaus, koska he saavat yhden tai useamman elektronin. |
| Sanojen alkuperä | Sana kationi on peräisin kreikan sanasta “kata”, joka tarkoittaa alaspäin. | Sana anion on peräisin kreikan sanasta “ano”, joka tarkoittaa alas. |
| Elektroni-protoni-suhde | Niillä on positiivinen varaus, koska protonien lukumäärä on suurempi kuin elektronien lukumäärä niissä | Niillä on negatiivinen varaus, koska elektronien lukumäärä on suurempi kuin protonien lukumäärä niissä. |
| Atomityyppi | Ne muodostuvat metallien atomeista | Ne muodostuvat epämetallien atomista. |
| Vetovoima elektrodien suhteen | Niitä vedetään negatiivisesti varautuneen elektrodin eli katodin kohdalla. | Niitä houkutellaan kohti positiivisesti varautunutta elektrodia, ts. Anodia. |
| Kuinka niitä merkitään | Niitä merkitään yläindeksillä + yhdisteen alkuaineen tai kemiallisen kaavan nimen jälkeen. | Niitä merkitään yläindeksillä - yhdisteen alkuaineen tai kemiallisen kaavan nimen jälkeen. |
| Säde | Kationien säde on pienempi, koska kiertoratojen lukumäärä pienenee elektronien menetyksen vuoksi | Anionien säde on suurempi kuin kationien säde, koska kiertoratojen lukumäärä kasvaa elektronien vahvistuksen myötä. |
| Kemiallinen reaktio | Kemiallisessa reaktiossa ne reagoivat anionien kanssa muodostaen ioniyhdisteitä | Kemiallisessa reaktiossa ne reagoivat kationien kanssa muodostaen ioniyhdisteitä. |
| Älä reagoi | Ne eivät vetoa tai reagoi positiivisesti varautuneiden hiukkasten kanssa | Ne eivät vetoa tai reagoi positiivisesti varautuneiden hiukkasten kanssa |
| esimerkit | Esimerkkejä kationeista voidaan antaa kuten rauta (Fe2 + ja Fe 3+), kalsium (Ca2 +), kalium (K +), alumiini Al3 +) ja ammoniumioni (NH4 +) jne. | Esimerkkejä anioneista voidaan antaa bromidina (Br-), kloridina (Cl-), nitridinä (N-) ja hydridinä (H-) jne. |
Mitä kationit ovat?
Kationit ovat positiivisesti varautuneita hiukkasia. Ne muodostuvat, kun elementin atomi menettää yhden tai useamman elektronin. Atomit tekevät niin saadakseen vakauden. Toisin sanoen he haluavat saada jalokaasujen järjestyksen, jotka ovat maailmankaikkeuden vakaimpia elementtejä. Sana kationi on peräisin kreikan sanasta “kata”, joka tarkoittaa alaspäin. Kationissa protonien lukumäärä on suurempi kuin elektronien. Kuten tiedämme, protoneilla on positiivinen varaus ja elektronilla negatiivinen varaus. Koska positiivisesti varautuneita hiukkasia on enemmän, kationeissa on positiivinen varaus. Kationit muodostuvat aina atomismetalleista. Syynä on, että metalleilla on taipumus menettää elektroneja. Metallipinnalla on lukematon määrä vapaita elektroneja. Siten metallit menettävät elektroneja, ja niiden atomit esiintyvät kationien muodossa.
Kationeja houkutellaan aina kohti katodia, joka on negatiivinen elektrodi. Kemiallisessa reaktiossa kationit reagoivat aina anionien kanssa muodostaen ioniyhdisteitä. Yksi paras esimerkki tämäntyyppisestä reaktiosta on tavallisen suolan, ts. Natriumkloridin (NaCl) muodostuminen, jossa natrium on kationi ja kloridi on anioni. Esimerkkejä kationeista voidaan antaa natriumina (Na +), kaliumina (K +), litiumina (Li +), magnesiumina (Mg2 +) ja alumiinina (Al3 +). Esimerkki positiivisesti varautuneista yhdisteistä on ammoniumioni (NH4 +).
Mitä anionit ovat?
Anionit ovat atomeja, joilla on negatiivinen varaus. Niillä on negatiivinen varaus, koska atomit saavat yhden tai useamman elektronin stabiilisuuden saavuttamiseksi. Siten elektronien lukumäärä tulee suuremmaksi kuin protonien lukumäärä noissa atomissa, ja ne osoittavat negatiivisen varauksen. Enimmäkseen ei-metallien atomit osoittavat tämän taipumuksen. Heillä on tällainen käyttäytyminen seuratakseen jalokaasuja, jotka ovat tämän maailmankaikkeuden vakaimpia elementtejä.
Anioneja houkutellaan aina kohti positiivista elektrodia, ts. Anodia. Kemiallisessa reaktiossa anionit reagoivat kationien kanssa muodostaen ioniyhdisteitä. Sana anion on peräisin kreikkalaisesta sanasta “ano”, joka tarkoittaa ylöspäin. Esimerkkejä anioneista voidaan antaa rikki (S-), jodidi-ioni (I-), bromidi (Br-), kloridi (Cl-), hydridi (H-) ja nitridi (N-).
Keskeiset erot
- Kationit ovat niitä hiukkasia, joilla on positiivinen varaus, kun taas anioita ovat hiukkasia, joilla on negatiivinen varaus.
- Kationilla on taipumus siirtyä kohti negatiivista elektrodia, ts. Katodiä, kun taas anioneilla on taipumus siirtyä kohti positiivista elektrodia, ts. Anodia.
- Kationeissa protoneja on enemmän kuin elektronia, kun taas anioneissa elektroneja on enemmän kuin protoneja.
- Kationit muodostuvat metallisten elementtien atomeista, kun taas anionit muodostuvat ei-metallisten elementtien atomista.
- Anionien kiertoradat ovat suurempia kuin kationien kiertoradat.
johtopäätös
Kationit ja anionit, molemmat ovat varautuneita hiukkasia. Luonnontieteiden opiskelijoille on erittäin tärkeää tuntea heidän eronsa. Yllä olevassa artikkelissa opimme selkeät erot kationien ja anionien välillä.